| Обучение и материалы |
|---|
| Физический справочник |
| Формулы по физике |
| Шпаргалки по физике |
| Энциклопедия |
| Репетиторы по физике |
| Работа для физиков |
| Быстрый устный счет |
| Виртуальные лабораторные |
| Опыты по физике |
| ЕГЭ онлайн |
| Онлайн тестирование |
| Ученые физики |
| Необъяснимые явления |
| Ваша реклама на сайте |
| Разное |
| Контакты |
| Спецкурс |
|---|
| Фейнмановские лекции |
|
В мире больших скоростей |
Введение в теорию относительности |
|
Лекции по биофизике |
| Лекции по ядерной физике |
| Ускорение времени... |
| Лазеры |
| Нанотехнологии |
| Книги |
| полезное |
|---|
| Смешные анекдоты о физике
Готовые шпоры по физике Физика в жизни Ученые и деньги Нобелевские лауреаты Фото Видео Карта сайта |
| На заметку |
|---|
| Если вам понравился сайт, предлагаем разместить нашу кнопку |
| Дополнительно |
|---|
|
Компьютерные программы по физике 
Физика и юмор 
Онлайн тестирование по физике 
|
Энтропия
Уравнение (44.7) или (44.12) может быть истолковано особо. При работе обратимых машин Q1/T1=Q2/T2, и тепло Q1 при температуре Т1 «эквивалентно» теплу Q2 при температуре Т2; ведь если поглощается Q1, то всегда выделяется тепло Q2. Если теперь придумать для Q/T особое название, то можно сказать, что при обратимых процессах поглощается столько же Q/T, сколько и выделяется. Иначе говоря, Q/T не убывает и не прибывает. Эта величина Q/T называется энтропией, и мы говорим, что «за обратимый цикл изменение энтропии равно нулю». Если T=1°, то энтропия равна Q/1°; мы уже снабдили энтропию особым символом S=Qs/1°. Энтропия повсюду обозначается буквой S, а численно она равна теплу (которое мы обозначили буквой Qs), выделяемому в одноградусном резервуаре (энтропия не равна просто теплу, это тепло, деленное на температуру, и измеряется она в джоулях на градус). Интересно, что, кроме давления, которое зависит от температуры и объема, и внутренней энергии (функции все тех же объема и температуры), мы нашли еще величину — энтропию вещества, которая тоже является функцией состояния. Постараемся объяснить, как вычислять энтропию и что мы понимаем под словами «функция состояния». Проследим за поведением системы в разных условиях. Мы уже умеем создавать разные условия экспериментально, например можно заставить систему расширяться адиабатически или изотермически. (Между прочим, машина не обязательно должна иметь только два резервуара, может быть и три, и четыре различные температуры, и машина будет обмениваться теплом с каждым из резервуаров.) Мы можем прогуляться по всей диаграмме pV, переходя от одного состояния к другому. Иначе говоря, можно перевести газ из состояния а в какое-нибудь другое состояние b и потребовать, чтобы переход из а в b был обратимым. Теперь предположим, что вдоль пути из а в b поставлены маленькие резервуары с разными температурами. Тогда каждый короткий шажок будет сопровождаться изъятием из вещества тепла dQ и передачей его в резервуар при температуре, соответствующей данной точке пути. Давайте свяжем все эти резервуары с помощью обратимых тепловых машин с одним резервуаром единичной температуры. После того как мы закончим перевод вещества из состояния а в состояние b, мы вернем все резервуары в их первоначальное состояние. Обратимая машина вернет каждую дольку тепла dQ, изъятого из вещества при температуре Т, и каждый раз при единичной температуре будет выделяться энтропия dS, равная
Подсчитаем полное количество выделенной энтропии. Разность энтропии, или энтропия, нужная для перехода из а в b в результате какого-нибудь обратимого изменения, это — полная энтропия, т. е. энтропия, взятая из маленьких резервуаров и выделенная при единичной температуре:
Поскольку мы не имеем права взять тепло из одноградусного резервуара, то при каждом путешествии из а в b приходится обходиться одним и тем же количеством энтропии. Это количество не зависит от пути, существенны только конечные точки. Таким образом, можно говорить о некоторой функции, которую мы назвали энтропией вещества. Эта функция зависит только от состояния вещества, т. е. только от объема и температуры. Можно найти функцию S(V, T). Мы подсчитаем изменение энтропии при обратимых изменениях вещества, следя за теплом, выделяемым в одноградусном резервуаре. Но это изменение можно выразить еще в терминах тепла dQ, изымаемого у вещества при температуре Т:
Полное изменение энтропии равно разности энтропии в конечной и начальной точках пути:
Это выражение не определяет энтропию полностью. Пока известна лишь разность энтропии в двух разных состояниях. Определить энтропию абсолютно можно только после того, как мы сумеем вычислить энтропию одного какого-нибудь состояния. Очень долго считалось, что абсолютная энтропия — это вообще ничего не значащее понятие. Но в конце концов Нернст высказал утверждение, названное им тепловой теоремой (иногда его называют третьим законом термодинамики). Смысл ее очень прост. Сейчас мы сообщим эту теорему, не объясняя, почему она верна. Постулат Нернста утверждает просто, что энтропия всякого тела при абсолютном нуле равна нулю. Теперь мы знаем, при каких Т и V (при T=0) энтропия равна нулю, и сможем вычислить энтропию в любой другой точке. Чтобы проиллюстрировать эту идею, давайте вычислим энтропию идеального газа. При изотермическом (а следовательно, обратимом) расширении ∫dQ/T равен просто Q/T, потому что Т постоянная. Таким образом, согласно (44.4), изменение энтропии равно
так что S(V, T)=NklnV плюс функция одной только температуры. А как S зависит от Т? Мы уже знаем, что при адиабатическом расширении теплообмена нет. Таким образом, энтропия остается постоянной, хотя объем V изменяется, заставляя изменяться Т (чтобы сохранить равенство TVγ-1=const). Ясно ли вам после этого, что
где а — постоянная, не зависящая ни от V, ни от T? [Постоянная а называется химической постоянной. Она зависит от свойств газа, и ее можно определить экспериментально в соответствии с теоремой Нернста. Для этого надо измерить тепло, выделяемое газом при его охлаждении и конденсации до превращения его при 0° в твердое тело (гелий и при этой температуре остается жидким). Потом надо найти интеграл ∫dQ/T . Можно найти а и теоретически; для этого понадобятся постоянная Планка и квантовая механика, но в нашем курсе этого мы не будем касаться.]
Мы уже знаем, что после обратимого цикла полная энтропия всего, что включается в процесс, не изменяется. Ведь тепло Q1, поглощенное при Т1, и тепло Q2, выделенное при Т2, вносят в энтропию равные по величине, но противоположные по знаку вклады. Поэтому чистое изменение энтропии равно нулю. Таким образом, при обратимом цикле энтропия всех участников цикла, включая резервуары, не изменяется. Это правило как будто похоже на закон сохранения энергии, но это не так. Оно применимо только к обратимым циклам. Если перейти к необратимым циклам, то закона сохранения энтропии уже не существует. Приведем два примера. Для начала предположим, что какая-то машина с трением производит необратимую работу, выделяя тепло Q при температуре Т. Энтропия возрастет на Q/T. Тепло Q равно затраченной работе, и когда мы производим какую-то работу с помощью трения о какой-то предмет, температура которого равна Т, то энтропия возрастает на величину W/ Т. Другой пример необратимости: если приложить друг к другу два предмета с разными температурами, скажем Т1 и Т2, то от одного предмета к другому перетечет некоторое количество тепла. Предположим, например, что мы бросили в холодную воду горячий камень. Насколько изменяется энтропия камня, если он отдает воде тепло ΔQ при температуре T1? Она уменьшается на ΔQ/T1. А как изменяется энтропия воды? Она возрастет на ΔQ/T1. Тепло, конечно, может перетечь только от более высокой температуры Т1 к более низкой Т2. Поэтому если Т1 больше T2, то ΔQ положительно. Таким образом, изменение энтропии положительно и равно разности двух дробей:
Итак, справедлива следующая теорема: в любом необратимом процессе энтропия всего на свете возрастает.Только обратимые процессы могут удержать энтропию на одном уровне. А поскольку абсолютно необратимых процессов не существует, то энтропия всегда понемногу растет. Обратимые процессы — это идеализированные процессы с минимальным приростом энтропии. К сожалению, нам не придется углубиться в область термодинамики. Наша цель лишь проиллюстрировать основные идеи этой науки и объяснить причины, по которым возможно основываться на этих аргументах. Но в нашем курсе мы не будем часто прибегать к термодинамике. Термодинамикой широко пользуются в технике и в химии. Поэтому с термодинамикой вы практически познакомитесь в курсе химии или технических наук. Ну а дублировать нет смысла, и мы ограничимся лишь некоторым обзором природы теории и не будем вдаваться в детали для специальных ее применений. Два закона термодинамики часто формулируют так: Это не слишком хорошая формулировка второго закона. В ней ничего не говорится, например, о том, что энтропия не изменяется после обратимого цикла и не уточняется само понятие энтропии. Просто это легко запоминаемая форма обоих законов, но из нее нелегко понять, о чем собственно идет речь. Все законы, о которых сейчас шла речь, мы собрали в табл. 44.1. А в следующей главе мы используем эту сводку законов, чтобы найти соотношение между теплом, выделяемым резиной при растяжении, и дополнительным натяжением резины при ее нагревании.
а) Если в систему обратимо втекает тепло ΔQ при температуре Т, то энтропия системы возрастает на ΔS = ΔQ/T. СМОТРИТЕ ТАКЖЕ:Социальные комментарии Cackle |
При использовании материалов сайта ссылка на www.all-fizika.com обязательна.



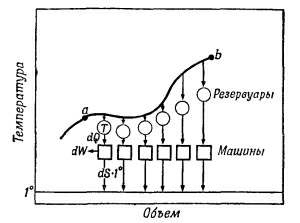 Вопрос заключается в том, зависит ли разность энтропии от пути в плоскости рV? Из а в b ведет много дорог. Вспомним, что в цикле Карно мы могли перейти из точки а в точку с (см. фиг. 44.6) двумя способами. Можно было расширить газ сначала изотермически, а потом адиабатически, а можно было начать с адиабатического расширения и окончить изотермическим. Итак, мы должны выяснить, меняется ли энтропия при изменении пути из а в b (фиг. 44.10). Она не должна измениться, потому что если мы совершим полный цикл, выйдя из а в b по одному пути и возвратясь по другому, то это путешествие будет эквивалентно полному циклу обратимой машины. При таком цикле никакого тепла не передается одноградусному резервуару.
Вопрос заключается в том, зависит ли разность энтропии от пути в плоскости рV? Из а в b ведет много дорог. Вспомним, что в цикле Карно мы могли перейти из точки а в точку с (см. фиг. 44.6) двумя способами. Можно было расширить газ сначала изотермически, а потом адиабатически, а можно было начать с адиабатического расширения и окончить изотермическим. Итак, мы должны выяснить, меняется ли энтропия при изменении пути из а в b (фиг. 44.10). Она не должна измениться, потому что если мы совершим полный цикл, выйдя из а в b по одному пути и возвратясь по другому, то это путешествие будет эквивалентно полному циклу обратимой машины. При таком цикле никакого тепла не передается одноградусному резервуару.
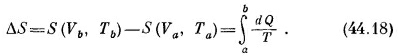
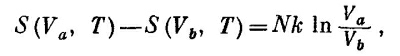
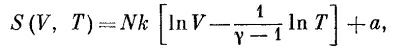
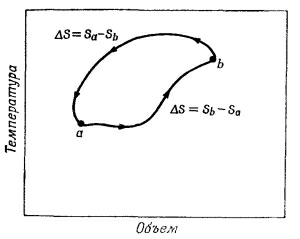 Отметим некоторые свойства энтропии. Сначала вспомним, что на участке обратимого цикла между точками а и b энтропия меняется на Sb— Sa (фиг. 44.11). Вспомним еще, что по мере продвижения вдоль этого пути энтропия (тепло, выделяемое при единичной температуре) возрастает в согласии с правилом dS=dQ/T, где dQ — тепло, изъятое из вещества при температуре Т.
Отметим некоторые свойства энтропии. Сначала вспомним, что на участке обратимого цикла между точками а и b энтропия меняется на Sb— Sa (фиг. 44.11). Вспомним еще, что по мере продвижения вдоль этого пути энтропия (тепло, выделяемое при единичной температуре) возрастает в согласии с правилом dS=dQ/T, где dQ — тепло, изъятое из вещества при температуре Т.
