| Обучение и материалы |
|---|
| Физический справочник |
| Формулы по физике |
| Шпаргалки по физике |
| Энциклопедия |
| Репетиторы по физике |
| Работа для физиков |
| Быстрый устный счет |
| Виртуальные лабораторные |
| Опыты по физике |
| ЕГЭ онлайн |
| Онлайн тестирование |
| Ученые физики |
| Необъяснимые явления |
| Ваша реклама на сайте |
| Разное |
| Контакты |
| Спецкурс |
|---|
| Фейнмановские лекции |
|
В мире больших скоростей |
Введение в теорию относительности |
|
Лекции по биофизике |
| Лекции по ядерной физике |
| Ускорение времени... |
| Лазеры |
| Нанотехнологии |
| Книги |
| полезное |
|---|
| Смешные анекдоты о физике
Готовые шпоры по физике Физика в жизни Ученые и деньги Нобелевские лауреаты Фото Видео Карта сайта |
| На заметку |
|---|
| Если вам понравился сайт, предлагаем разместить нашу кнопку |
| Дополнительно |
|---|
|
Компьютерные программы по физике 
Физика и юмор 
Онлайн тестирование по физике 
|
Бойля-Мариотта законБойля-Мариотта закон, один из основных газовых законов, согласно которому при постоянной температуре Т объём V данной массы газа обратно пропорционален его давлению р, pV=const (рис.). Установлен английским учёным Р. Бойлем (R. Boyle) в 1662, в 1676 сформулирован также французским физиком Э. Мариоттом (Е. Mariotte). Строго выполняется только для идеального газа. Для реальных газов, объёмом молекул и межмолекулярным взаимодействием которых пренебречь нельзя, Бойля-Мариотта закон выполняется приближённо — тем лучше, чем дальше от критического состояния находится газ. Бойля-Мариотта закон описывает изотермический процесс в газе и следует из кинетической теории газов.
|
© All-Физика, 2009-2026
При использовании материалов сайта ссылка на www.all-fizika.com обязательна.
При использовании материалов сайта ссылка на www.all-fizika.com обязательна.

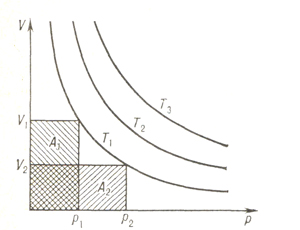 Зависимость объёма V от давления р постоянной массы газа при температуpax T1<T2<T3. Изотермы T1, T2, T3 имеют вид равносторонних гипербол, площади А1 и А2 равны.
Зависимость объёма V от давления р постоянной массы газа при температуpax T1<T2<T3. Изотермы T1, T2, T3 имеют вид равносторонних гипербол, площади А1 и А2 равны.